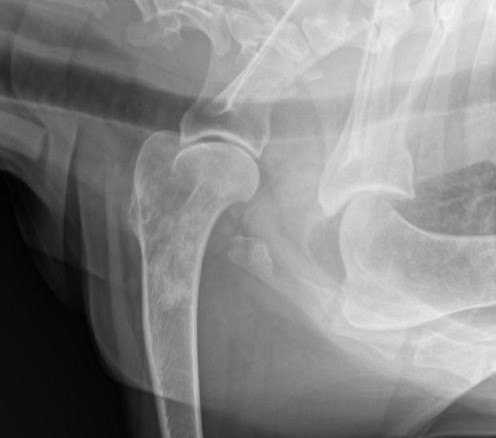
El osteosarcoma (OSA) apendicular es el tumor primario de hueso más común en la especie canina. Es un tumor mesenquimatoso maligno de células óseas primitivas, estas células producen una matriz extracelular de osteoide. Osteosarcoma.
Representa hasta el 85% de las neoplasias que se originan en el esqueleto, la demografía ha sido bien informada, es en gran parte una enfermedad de perros de mediana edad, con una edad promedio de presentación de 7 años. La proporción total de machos y hembras con osteosarcoma parece ser bastante parecida, con una incidencia ligeramente mayor en los machos.
El aumento de peso y más específicamente la altura, parecen ser los factores más predictivos de la enfermedad en los caninos. Las razas de mayor riesgo son San Bernardo, Gran Danés, Setter Irlandés, Dóberman pinscher, Rottweiler, Pastor alemán y Golden retriver. Sin embargo, el tamaño parece ser un factor más importante que la raza.
En general, se desconoce la etiología del osteosarcoma canino. Una teoría simplista propone que en perros grandes y de rápido crecimiento pueden producirse múltiples traumatismos menores y la posterior lesión de las células sensibles de la región epifisaria. Esto puede iniciar la enfermedad al inducir señales mitogénicas que aumentan la probabilidad de que se desarrolle un linaje mutante y la posterior formación de tumores. Existen reportes de OSA asociado a implantes metálicos utilizados para reparación de fracturas, osteomielitis crónica y con fracturas en las que no se utilizó reparación interna.
Aproximadamente el 75% de los osteosarcomas ocurren en el esqueleto apendicular (miembros), y el resto ocurre en el esqueleto axial (cráneo, vertebras, costillas y esternón). Las extremidades anteriores se ven dos veces más afectadas que los miembros posteriores.
Existen muchas subclasificaciones histológicas de OSA basadas en el tipo y la cantidad de matriz y características de las células, que incluyen: OSA osteoblástico, condroblástico, fibroblástico, pobremente diferenciado y telangiectásico (un subtipo vascular). En caninos, no está bien establecido que exista una diferencia en el comportamiento biológico de las diferentes subclasificaciones histológicas; sin embargo, el grado histológico, basado en características microscópicas, puede predecir el comportamiento sistémico.
OSA tiene efectos locales muy agresivos y causa lisis o producción de hueso. La enfermedad local suele ir acompañada de inflamación de los tejidos blandos. Puede producirse una fractura patológica del hueso afectado. En raras ocasiones, OSA atravesará la superficie de una articulación.
Los perros con OSA, en los miembros, generalmente presentan cojera y/o hinchazón en el sitio primario. A veces, hay antecedentes de traumatismo leve justo antes de la aparición de la cojera y, a menudo, esto puede dar lugar a un diagnóstico erróneo de otra lesión ortopédica. Es probable que el dolor se deba a microfracturas o rotura del periostio inducida por osteólisis del hueso cortical con extensión tumoral desde el canal medular. A medida que la cojera empeora, puede surgir una hinchazón moderadamente firme a blanda y dolorosa variable en el sitio primario.
Aunque menos del 15% de los perros presentan metástasis ósea o pulmonar detectable radiográficamente en el momento de la presentación, aproximadamente el 90% morirá con enfermedad metastásica, generalmente en los pulmones.
La metástasis por vía hematógena es más común, pero en raras ocasiones puede ocurrir extensión a los ganglios linfáticos regionales. Aunque el pulmón es el sitio principal de metástasis, la diseminación del tumor a los huesos u otros sitios de tejidos blandos ocurre con cierta frecuencia.
La enfermedad metastásica oculta está presente en aproximadamente el 90% de los perros en el momento de la presentación y la supervivencia media es sólo de 3 a 4 meses si la amputación es el único tratamiento; por lo tanto, es necesaria alguna forma de terapia sistémica (quimioterapia) para mejorar la supervivencia. Sin ningún tratamiento, la afección se vuelve muy dolorosa debido a la extensa destrucción del hueso y el tejido circundante por los tumores primarios y la mayoría de los propietarios optan por la eutanasia para sus mascotas poco después del diagnóstico si no se les puede ofrecer ningún tratamiento.
La amputación de la extremidad afectada es el tratamiento estándar para OSA apendicular canino. Incluso los perros de razas grandes y gigantes pueden funcionar bien después de la amputación de una extremidad y la mayoría de los propietarios están satisfechos con la movilidad y la calidad de vida de las mascotas después de la cirugía. La enfermedad articular degenerativa preexistente en la mayoría de los perros mayores de razas grandes, rara vez es una contraindicación para la amputación. La mayoría de los perros lo compensarán fácilmente, esto rara vez resulta en un problema clínico.
En general, se recomienda realizar una amputación completa del cuarto delantero para las lesiones de las extremidades anteriores y una amputación por desarticulación coxofemoral para las lesiones de las patas traseras. Este nivel de amputación asegura la eliminación completa de la enfermedad local y también da resultado más cosmético y funcional, cuanto más agresiva es la amputación, se reduce el peso que debe soportar el paciente.
La cirugía por sí sola debe considerarse paliativa para pacientes con osteosarcoma. Se recomienda completar la paliación dando adyuvancia con quimioterapéuticos, se utilizan compuestos del platino solo o combinado con antraciclinas.
Parte importante del manejo clínico de estos pacientes es controlar el dolor que puede llegar a ser mal adaptativo en la mayoría de los casos, por lo que siempre en sus protocolos se combina con terapia analgésica utilizando antiinflamatorios no esteroidales de forma crónica combinados con derivados de opiáceos, muchas veces es necesario utilizar agentes anticonvulsivos con efectos analgésicos como parte del manejo.
Fuentes consultadas
Dobson M, Jane (2011). Segunda edición. BSAVA Manual of canine and feline Oncology. Pp 142-144.
Henry J, Carolyn (2010). Cancer Management in small Animal Practice. Pp 317, 318.
Withrow J. Stephen (2013). Quinta edición. Small Animal Clinical Oncology. Pp 335 y 337.